 TuttoChimica.it
TuttoChimica.it
Chimica, laboratorio e dintorni...

Spettrofotometro
Principi di funzionamento e motodi di analisi
Lo spettrofotmetro è uno strumento in gradi di effettuare analisi quali-quantitative utilizzando una sorgente luminosa. Le onde elettromagnetiche, a seconda della frequenza e relativa lunghezza d'onda, vengono suddivise secondo il cosiddetto spettro elettromagnetico:
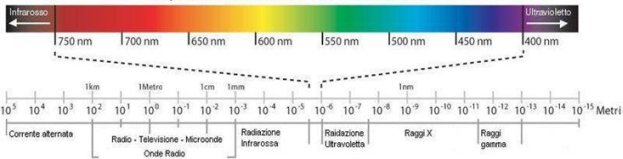
Di queste radiazioni siamo in grado di vederne coi nostri occhi solo un ristretto campo, all'incirca tra 750 nm e 400 nm, il cosiddetto 'spettro visibile'. La luce proveniente dal sole contiene non solo frequenze del visibile ma anche altre, per esempio UV e raggi infrarossi. Quando la luce colpisce un oggetto, lo possiamo vedere di un certo colore: questo è dovuto al fatto che le componenti di quell'oggetto, o i pigmenti che lo ricoprono, sono in grado di assorbire determinate frequenze, mentre altre vengono respinte (riflesse) e giungono ai nostri occhi. Un oggetto rosso assorbirà quindi le frequenze del blu/viola e rifletterà quelle del giallo/rosso, un oggetto nero è in grado di assorbire tutte le radiazioni dello spettro visibile mentre uno bianco le riflette tutte.
Lo spettrofotometro utilizza proprio questa capacità della luce di essere assorbita, a diverse frequenze, dalle sostanze chimiche o biologiche. Lo strumento è costituito da diverse parti schematizzabili nella seguente figura:
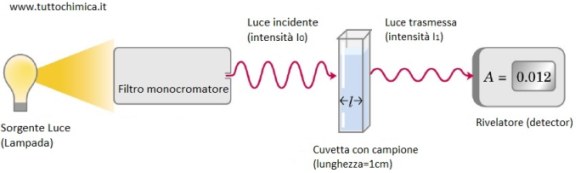
Una sorgente di luce, generalmente nell'UV/visibile, genera la luce che viene filtrata da un monocromatore in grado di lasciar passare una singola lunghezza d'onda. Nello strumento l'impostazione della lunghezza d'onda di utilizzo viene effettuata generalmente in via digitale tramite in pannello elettronico dello strumento. Questa radiazione passa attraverso l'alloggiamento dello strumento in cui viene posto il campione, all'interno di una provetta particolare chiamata cuvetta. Le cuvette possono essere prodotte con plastiche particolari in grado di lasciar passare le radiazioni tra 300 e 1000 nm, oppure anche più costose in quarzo, che risulta trasparente alla radiazione anche nell'intervallo 200-300 nm.


Spettrofotometro e cuvetta
Il raggio luminoso, se di lunghezza d'onda opportuna, passando attraverso il campione sarà in parte assorbito, pertanto il raggio incidente e raggio trasmesso avranno intensità luminose differenti (ma stessa frequenza e lunghezza d'onda). Il raggio termina il suo percorso in un detector in grado di valutare l'intensità della radiazione che vi arriva. Lo strumento è in grado di determinare un parametro, l'Assorbanza, definita come:
A= log (I0/I1)
essendo I1 e I0 le intensità di luce trasmessa e iniziale. L'assorbanza è un numero senza unità di misura, che dunque avrà valore 0 quando I1=I0, avrà valore 2 quando la luce trasmessa è un centesimo della luce incidente (log[100/1]) e così via. Generalmente gli spettrofotometri più comuni riescono a leggere nel campo di assorbanze tra 0 e 2, mentre per riuscire a determinare valori maggiori di assorbanza servono strumenti molto più sensibili.
L'assorbanza segue la legge principe della spettrofotometria, la legge di Lambert e Beer secondo la quale Assorbanza e concentrazione del campione in cuvetta sono linearmente dipendenti.
A= ε c l
dove c è la concentrazione molare (M) della sostanza nella cuvetta, l la lunghezza della cuvetta in cm, e ε il coefficiente di estinzione molare (espresso quindi in M-1cm-1), una costante caratteristica per ogni sostanza (varia a seconda della lunghezza d'onda incidente e indica la capacità di quella sostanza di assorbire quella radiazione) e l il cammino ottico, cioè la lunghezza della cuvetta in cm. Generalmente questa è standardizzata in 1 cm per lato, pertanto può essere trascurata nella formula.
Parte della componente luminosa potrebbe essere bloccata o dispersa in ogni caso anche dalla cuvetta vuota o dal solvente utilizzato, pertanto lo strumento viene in genere tarato a zero di assorbanza (questo è chiamato 'fare il bianco') mediante un apposito pulsante lasciando all'interno dello strumento la cuvetta vuota o la cuvetta con il solo solvente.
Molti spettrofotometri sono impostabili su una lunghezza d'onda per volta ed effettuano letture singole di assorbanza a una specifica lunghezza d'onda. Esistono anche spettrofotometri 'a doppio raggio' che presentano due alloggiamenti, uno per la cuvetta del campione e uno per la cuvetta del bianco che viene sottratto in automatico al campione. Ci sono poi spettrofotometri a serie di diodi in gradi di effettuare in pochi secondi una lettura di tutte le assorbanze del campione comprese in un range di lunghezze d'onda (in genere UV/visibile). Il risultato di questo secondo tipo di strumento è lo 'spettro di assorbimento' di una specifica sostanza, per le clorofile e i carotenoidi gli spettri sovrapposti delle differenti sostanze per esempio risultano i seguenti:
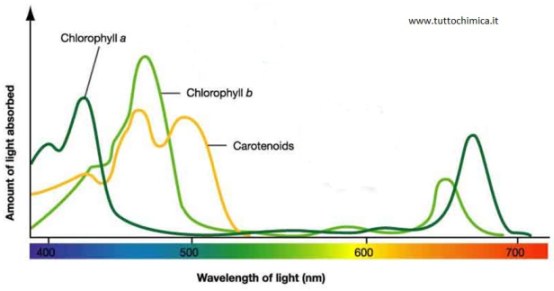
Una molecola può quindi assorbire in punti differenti dello spettro generando curve di assorbimento dotate di picchi massimi e zone dove non vi è assorbimento, per esempio le varie clorofille assorbono attorno a 430-480 e 660 nanometri e quindi nelle zone del blu e del rosso (risultando infatti del caratteristico colore verde che non è assorbito).
Analisi allo spettrofotometro:
Lo spettrofotometro è
uno strumento molto utilizzato per determinazioni quantitative, essendo l'assorbanza
correlabile a [c] secondo la legge di Lambert Beer. La prima cosa da
fare, qualora per la sostanza in esame non si conosca già il
coefficiente di estinzione molare che spesso si trova tabulato, è
costruire una retta di taratura tra Assorbanza e Concentrazione. E'
sufficiente preparare una serie di concentrazioni note della sostanza in
analisi
pura e disciolta in un solvente (acqua, alcool, solventi organici...),
fare il bianco (azzeramento dell'assorbanza) con la cuvetta piena del
solo solvente e quindi leggere le assorbanze delle varie concentrazioni
note ponendo le rispettive cuvette nello strumento una dopo l'altra. La retta
risultante tra Assorbanza sulle ordinate e Concentrazione (espressa per
es. in mg/ml) in ascisse sarà di questo tipo:
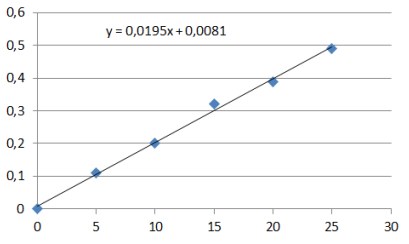
A questo punto per determinare la concentrazione incognita del campione in analisi basterà prepararne una diluizione nello stesso solvente, determinare il valore di Assorbanza e, grazie alla retta creata con gli standard noti, ricavare il relativo valore di concentrazione (considerando eventuali fattori di diluizione usati).
Categorie Articoli e Appunti
• Chimica Generale
•
Chimica Analitica
•
Chimica Inorganica
•
Chimica Organica
•
Biochimica
•
Biologia
•
Genetica