 TuttoChimica.it
TuttoChimica.it
Chimica, laboratorio e dintorni...

Struttura e proprietà dell'acqua
Struttura molecolare, caratteristiche
L'acqua è la molecola essenziale per la vita biologica sul nostro pianeta, ed è dotata di caratteristiche che le conferiscono particolari ed uniche proprietà.
Partiamo dalla struttura molecolare dell'acqua, che sappiamo avere formula H2O. L'atomo di ossigeno ha configurazione elettronica 1s2 2s2 2p4 con due orbitali p aventi quindi un singolo elettrone. Prima di legarsi ai due atomi di idrogeno (1s1) l'ossigeno subisce una ibridazione di tipo sp3, cioè l'orbitale 2s e gli orbitali 2p si fondono insieme dando origine a 4 orbitali ibridi sp, dalla forma di un 8 con un lobo piccolo e un lobo maggiore che si dispongono nello spazio a simmetria tetraedrica:
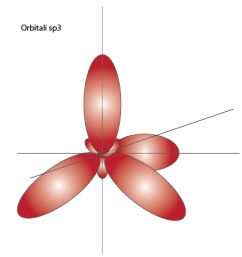
Due di questi orbitali posseggono due elettroni e sono quindi completi, gli altri due hanno un solo elettrone, e si legheranno per completarsi con gli orbitali 1s degli idrogeni, formando due legami covalenti separati fra loro da un angolo di 104°5'.
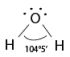
Poichè l'atomo di Ossigeno è molto più elettronegativo deglia tomi di idrogeno, risulterà una delocalizzazione parziale di carica negativa sull'ossigeno, e positiva sui protoni, con risultato di una molecola molto polare e che potrà facilmente sviluppare legami a idrogeno intermolecolari.
Questa polarità è la principale responsabile delle caratteristiche chimico-fisiche dell'acqua, per esempio:
1) il forte potere solvente dell'acquaa specialmente nei confronti di sostanze ioniche;
2) il fenomeno della tensione superficiale dell'acqua. Basta notare una goccia d'acqua per rendersi conto di questo fenomeno: le molecola di acqua superficiali risultano più fortemente attratte verso il basso dalle molecole di acqua sottostanti, creando una specie di 'pellicola' che consente per esempio all'acqua contenuta in un bicchiere di riempirlo e superarne leggermente il bordo senza traboccare fuori. Inoltre la tensione superficiale è responsabile della forma sferica delle gocce d'acqua.
3) I forti legami a idrogeno sono responsabili anche dell'elevato
punto di ebollizione (100°C) e punto di congelamento (0°C). L'acqua
presenta calore latente di fusione di 79,7 KCal/Kg e calore latente di
ebollizione di 539,55 KCal/Kg, valori piuttosto elevati.
Categorie Articoli e Appunti
• Chimica Generale
•
Chimica Analitica
•
Chimica Inorganica
•
Chimica Organica
•
Biochimica
•
Biologia
•
Genetica